El Motor de Diseño de Fármacos de Isomorphic Labs abre una nueva frontera más allá de AlphaFold
Abriendo una nueva ventana para los biológicos complejos
Pero las moléculas pequeñas (como la aspirina) son solo una pieza del rompecabezas. A medida que las modalidades terapéuticas se expanden hacia biológicos complejos (como la insulina), la capacidad para modelar con precisión las interfaces anticuerpo-antígeno es fundamental.
IsoDDE proporciona un cambio progresivo en la precisión para este dominio. Supera a AlphaFold 3 en 2,3 veces y a Boltz-2 en 19,8 veces en el régimen de alta fidelidad (DockQ > 0,8) en un conjunto de pruebas de anticuerpos y antígenos novedoso y desafiante.
De forma crucial, IsoDDE muestra un rendimiento notable en el bucle CDR-H3 —la parte más variable y difícil de predecir de un anticuerpo—, desbloqueando efectivamente nuevas posibilidades para el diseño de anticuerpos de novo.
Un nuevo estándar de oro para la predicción de afinidad de unión
Conocer la estructura 3D de un sistema bioquímico es solo el primer paso; La optimización eficaz de fármacos requiere saber cuán fuerte se unirá una molécula a su objetivo.
Los enfoques tradicionales están limitados al espacio químico similar a los datos de entrenamiento o por su alto coste computacional y dificultad de ejecución (por ejemplo, enfoques basados en física). Más recientemente han surgido métodos basados en aprendizaje profundo que aportan nueva velocidad a esta tarea, pero aún están por detrás de los enfoques basados en física en cuanto a precisión.
IsoDDE supera por un margen considerable a todos los métodos de aprendizaje profundo en tres benchmarks públicos: FEP+ 4, OpenFE y la reciente tarea de predicción de afinidad de enlace ciego CASP16.
De hecho, sorprendentemente, IsoDDE puede superar el rendimiento de métodos basados en física como el FEP, a pesar de que estos requieren fundamento en estructuras cristalinas experimentales y que IsoDDE no.
Al ofrecer predicciones de afinidad de unión altamente precisas a gran velocidad, IsoDDE permite a los investigadores clasificar y optimizar rápidamente moléculas potenciales a través de diversas series químicas durante los programas de diseño de fármacos.
Expansión del proteoma ligandable
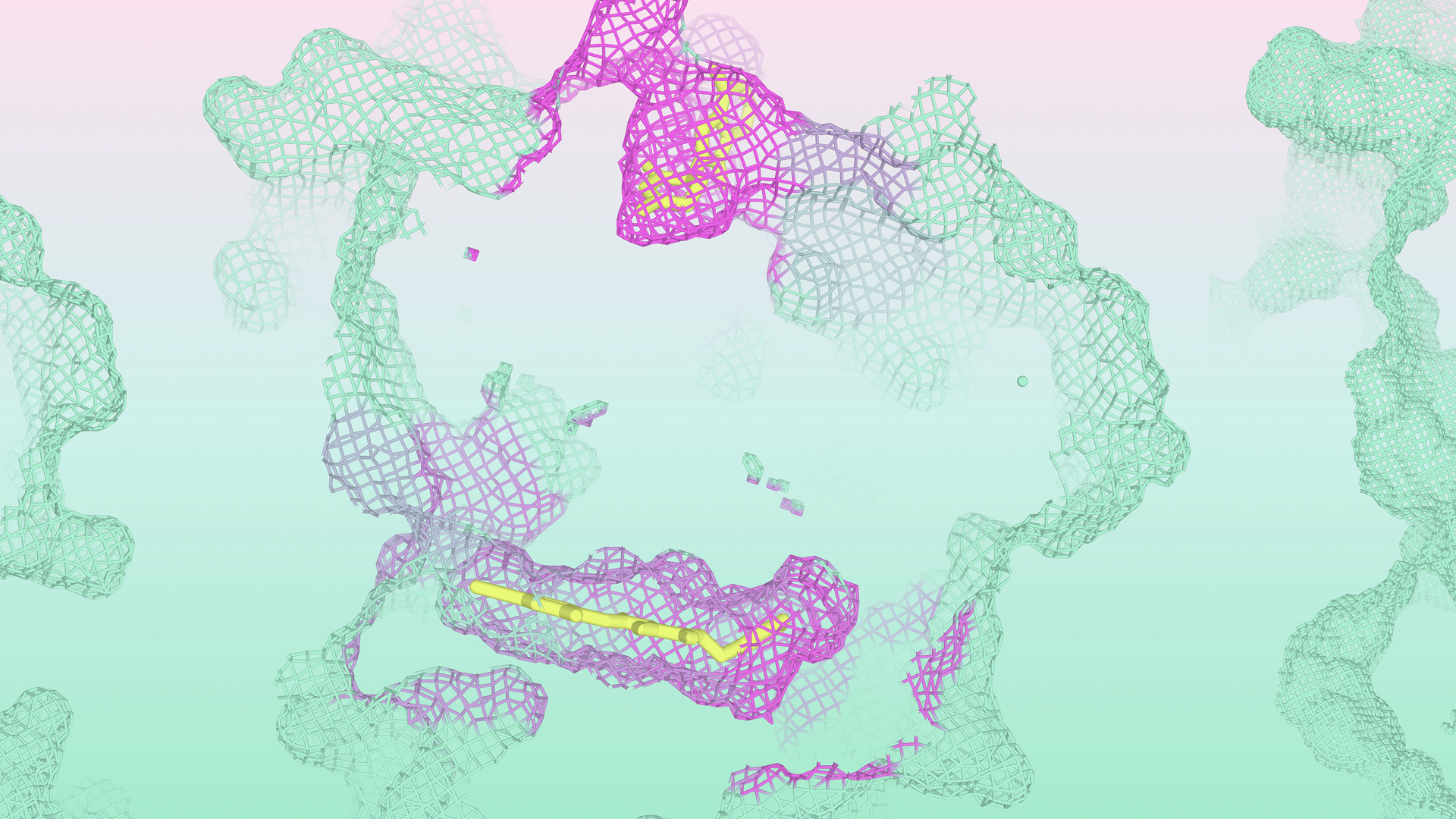
La capacidad de identificar todos los bolsillos potenciales de una proteína, en ausencia de un ligando conocido, abre una serie de oportunidades únicas. Ya sea tratando con un objetivo de descubrimiento de fármacos de primer nivel sin anotación estructural o buscando una forma novedosa de modular una proteína bien estudiada, una capacidad general de identificación de bolsillos puede utilizarse para revelar el conjunto completo de posibles mecanismos de acción a seguir para el diseño molecular.
IsoDDE muestra la capacidad de identificar bolsillos nuevos y ligandoables incluso en ausencia de un ligando conocido y lejos del conjunto de entrenamiento del modelo. Esta capacidad para la identificación 'ciega' demuestra niveles de rendimiento que se acercan a técnicas experimentales como el remojo de fragmentos, que requieren grandes inversiones de tiempo, costes significativos y trabajo experimental en el mundo real. En comparación, IsoDDE se ejecuta en un ordenador en cuestión de segundos.
Podemos ver el poder de esta capacidad en el ejemplo del cereblon —un receptor de sustrato para el complejo ligasa CRL4 E3— que desempeña un papel clave en el marcado de proteínas dañadas o mal plegadas para la degradación proteasomal. Durante los últimos 15 años, se creía que existía una forma principal de drogar el cerebro: a través del clásico bolsillo de unión a la talidomida. Sin embargo, un estudio reciente (Dippon et al. 2026) descubrió experimentalmente un bolsillo de unión novedoso que era tanto alostérico (alejado del sitio tradicional de unión) como críptico (oculto en ausencia de un ligando de unión).
IsoDDE pudo recapitular el descubrimiento de este bolsillo, prediciendo la ubicación tanto de los sitios crípticos conocidos como de los novedosos usando solo la secuencia de cereblones como entrada, sin especificar la identidad de los ligandos. Además, una vez especificados los ligandos, IsoDDE pudo plegarlos correctamente en sus respectivos bolsillos en la orientación correcta.
Avanzando en el descubrimiento de fármacos
IsoDDE representa un salto adelante en precisión y capacidad, aportando una comprensión más profunda a las máquinas moleculares que componen el cuerpo humano y avanzando en el proceso de diseño de fármacos para modularlas.
Nuestros equipos dedicados al diseño de fármacos en Isomorphic Labs utilizan estas capacidades cada día en nuestros programas: para comprender estructuras invisibles, identificar bolsillos no caracterizados y crear materia química novedosa en la búsqueda de nuevos medicamentos para los pacientes.
Esperamos seguir explorando las fronteras del diseño de fármacos in silico y poner nuestras nuevas capacidades más potentes en objetivos de fármacos históricamente desafiantes.
Agradecemos a nuestros amigos de Google DeepMind por sus discusiones productivas y la colaboración.
Por favor, utiliza la siguiente cita si haces referencia a esta obra:





No hay comentarios:
Publicar un comentario