1-No, Pfizer no ha ocultado al mundo un fármaco que cura o previene el alzhéimer (I)
Si todo lo que se está publicando y tuiteando hoy fuera cierto, sería un día histórico para la humanidad: este 6 de junio de 2019 tendríamos por fin un fármaco para curar y prevenir el alzhéimer.
Es decir, que una vez desaparecido todo el revuelo de los juicios de
valor sobre las prácticas empresariales de Pfizer, lo que quedaría de
todo ello sería una noticia de inmensa trascendencia: la cura del
alzhéimer.
Solo que no es cierto. Pfizer no tiene un fármaco que cura el
alzhéimer. Pfizer no tiene un fármaco que previene el alzhéimer. Pfizer
no ha ocultado al mundo que tiene un fármaco que cura ni previene el
alzhéimer; en primer lugar, porque no lo tiene, y en segundo lugar, porque no hay nada oculto:
este fármaco es de sobra conocido desde hace años por la comunidad
científica, que ya ha estado valorando su potencial contra el alzhéimer
sin necesidad de que Pfizer revele o deje de revelar nada.

Imagen de Pixabay.
Por lo tanto, hoy no es día de buenas noticias, sino de malas. La
primera mala noticia es que la cura del alzhéimer sigue sin existir; si
es que puede llamarse noticia a algo que continúa no siendo, tal como no
lo era ayer. Lo que sí es seguro una mala noticia es que lo ocurrido hoy es un triunfo más de la desinformación y la demagogia.
 Esta es la desinformación y demagogia que circula: Pfizer creó un fármaco del que sabe que cura o previene el alzhéimer, y lo enterró para que nadie lo utilizara porque le resulta más rentable que la gente siga enferma.
Esta es la desinformación y demagogia que circula: Pfizer creó un fármaco del que sabe que cura o previene el alzhéimer, y lo enterró para que nadie lo utilizara porque le resulta más rentable que la gente siga enferma.
Y esta es la información: existe un fármaco creado por investigadores
básicos, ampliamente conocido y que se emplea en el tratamiento de la
artritis reumatoide. Desde hace años, la comunidad científica piensa que
los fármacos de este tipo quizá podrían aportar algún beneficio contra
el alzhéimer. De hecho, se han hecho diversos estudios sobre ello, sin que aún exista una pista clara sobre su posible utilidad.
Con el tiempo, han surgido otros fármacos biosimilares (casi idénticos,
con el mismo efecto). Pfizer, que vende el fármaco original, se planteó
si emprender un ensayo clínico a gran escala. Decidió no hacerlo. Con
independencia de las explicaciones que Pfizer pueda ofrecer o haya
ofrecido al respecto, existen razones perfectamente comprensibles para
que una compañía decida no abordar un enorme gasto de resultados
inciertos sobre un fármaco cuyas patentes están expirando, que otras
entidades pueden ensayar libremente y del que además ya existen otros
clones sometidos a investigaciones y a disposición de la comunidad
científica.
Y ahora, la versión larga, por si a alguien le interesa conocer la verdad entre tanto espumarajo.
En 1991, el equipo dirigido por Bruce Beutler en el University of Texas Southwestern Medical Center publicó la creación de una proteína quimérica
(formada por la unión de trozos de otras) compuesta por el receptor del
factor de necrosis tumoral alfa (TNF-α) y un fragmento de anticuerpo.

Estructura del etanercept. Imagen de NEUROtiker / Wikipedia.
El TNF-α es una molécula producida por el organismo que promueve los
procesos inflamatorios. La proteína quimérica tenía por objeto inhibir
la acción del TNF-α in vivo, uniéndose a este y secuestrándolo
para neutralizar su función. Dado que ciertas enfermedades como las
autoinmunes producen sus síntomas a través de una activación incorrecta
del sistema inmunitario, en la que el TNF-α desempeña un papel
relevante, la idea de Beutler y sus colegas era que la molécula por
ellos diseñada podía sumarse a otras opciones disponibles en el
tratamiento de dichas dolencias. Los experimentos mostraron que la proteína bloqueaba eficazmente la acción del TNF-α.
Los investigadores patentaron su molécula y vendieron los derechos a la compañía biotecnológica Immunex, que en 1998 desarrolló el producto para el tratamiento de la artritis reumatoide.
Su nombre es etanercept, y su marca comercial Enbrel. En 2002 Immunex
fue absorbida por Amgen, que actualmente vende el etanercept en EEUU. En
el resto del mundo (excepto Japón) la comercialización del fármaco
corría a cargo de Wyeth, que en 2009 fue adquirida por Pfizer.
Desde entonces, el etanercept se ha venido utilizando para el tratamiento de la artritis reumatoide y otras enfermedades autoinmunes, no sin problemas:
tanto este fármaco como otros similares son, por su propia definición,
inmunosupresores, lo que ha llevado a que ciertos pacientes contraigan
infecciones graves e incluso mortales.
Por otra parte, entra el alzhéimer, una enfermedad para la que no
existe cura ni prevención y cuya causa primaria aún se ignora. Desde
hace años se sabe que el cuadro inflamatorio forma parte del conjunto de
síntomas del alzhéimer, pero sin que aún se conozca qué relevancia
tiene este proceso en el desarrollo de la enfermedad. La posibilidad de
que la inflamación pudiera ser un factor primario es solo una de las
hipótesis que circulan en torno a la patología del alzhéimer, pero los
investigadores consideran la posibilidad de que el tratamiento
del cuadro inflamatorio pueda ayudar a paliar los síntomas o frenar su
progresión.
Por ello, desde hace años los investigadores han comenzado a ensayar
la posible acción de varios fármacos antiinflamatorios contra el
alzhéimer, comenzando por los modelos animales. Uno de estos fármacos es el etanercept.
La patente del fármaco expiró en Europa en 2015, mientras que en EEUU
aún estará vigente hasta 2028 porque Amgen consiguió una extensión. En
la práctica, esto implica que cualquier compañía puede producir
etanercept fuera de EEUU. Incluso en aquel país, cualquier compañía
puede producir otros inhibidores biosimilares, aunque probablemente
(como de hecho ha ocurrido) se enfrente a demandas por parte de Amgen.
Lo que debe quedar claro con esto es que el etanercept, ni jamás ha
sido secreto, ni jamás ha sido único, ni pertenece ya siquiera a Pfizer.
Está publicado desde 1991, pertenece ya al dominio público (excepto en
EEUU) y existen numerosas alternativas, desde los más generales
antiinflamatorios no esteroideos hasta los más específicos inhibidores
de TNF-α y, dentro de estos, los biosimilares; actualmente existe casi una veintena de fármacos biosimilares al etanercept en distintas fases de desarrollo y comercialización.
Y como es obvio, siendo un fármaco común –de hecho uno de los
antiinflamatorios más vendidos del mundo–, tampoco ha estado guardado en
un armario o en una caja fuerte. Mañana continuaremos contando qué dicen los ensayos emprendidos hasta ahora con este fármaco contra el alzhéimer,
qué es lo que Pfizer sabía y no dijo, qué relevancia real tenía esto, y
cómo un dato no científico en un Power Point que llega a manos de un
periodista puede pintarse de amarillo para convertirse en una de las fake news más sonadas del momento.
https://culturacientifica.com/2019/06/13/piensa-bien-y-acertaras-los-casos-de-pfizer-e-isdin/?fbclid=IwAR0NATcCDAq4v59WJST0EN8JzmdRcqW-d7ql-DThbFEfry6FCsRq1JAZqjs
2.No, Pfizer no ha ocultado al mundo un fármaco que cura o previene el alzhéimer (II)
Como comencé a explicar ayer,
desde hace años los investigadores han planteado la posibilidad de que
los inhibidores de citoquinas proinflamatorias (moléculas que produce el
cuerpo y que promueven la respuesta de inflamación contra las
agresiones al organismo) podrían ser útiles en la lucha contra el alzhéimer, ya que la inflamación es uno de los síntomas de la enfermedad.
Sin embargo, y como también conté ayer, en realidad el
proceso patológico del alzhéimer aún es desconocido, por lo que la
inflamación podría no ser una causa, sino un efecto. De ser
así, atacar la inflamación contra el alzhéimer sería como luchar contra
un terremoto protegiendo la cristalería: se evitará que se rompan las
copas y los vasos, pero nada más.
Es más, hasta tal punto se desconoce la patogénesis del alzhéimer que ni siquiera puede descartarse del todo que esta inflamación sea en realidad beneficiosa.
Aunque la inflamación crónica suele tener efectos nocivos, en su origen
es una respuesta del organismo contra una agresión. En el caso del
alzhéimer, se ha propuesto incluso que la activación de la microglía (el
sistema inmune propio del cerebro) podría ayudar a eliminar las placas
de proteína beta-amiloide que tradicionalmente se han asociado con la
muerte neuronal en los pacientes de alzhéimer.
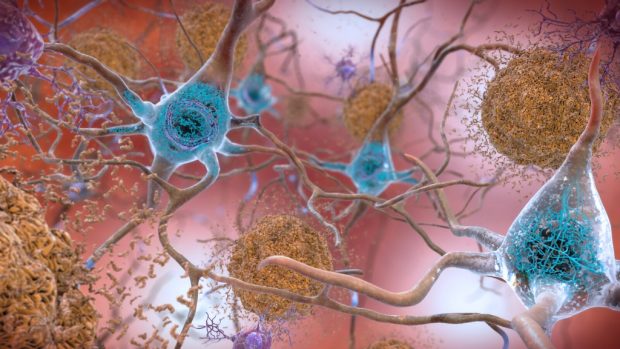
Ilustración
de anomalías neuronales en el alzhéimer: placas beta-amiloides (marrón)
y ovillos neurofibrilares (azul). Imagen de NIH.
El primer estudio piloto que evaluó el uso del etanercept de Amgen y Pfizer contra el alzhéimer se publicó en 2006,
cuando el fármaco llevaba ya utilizándose contra la artritis reumatoide
durante ocho años en EEUU, seis en Europa. En aquella ocasión,
investigadores de la Universidad de California dirigidos por Edward
Tobinick trataron a 15 pacientes de alzhéimer durante seis meses
mediante inyecciones de etanercept en la médula espinal.
Al término del pequeño estudio, los investigadores observaron mejoras
en los resultados de los test cognitivos de los pacientes. Esta fue su
conclusión: “Un creciente volumen de ciencia básica y evidencias
clínicas implica a los procesos inflamatorios y la resultante activación
glial en la patogénesis del alzhéimer. Este pequeño estudio piloto
sugiere que la inhibición de la citoquina inflamatoria TNF-α puede ser prometedora como enfoque potencial para el tratamiento del alzhéimer. Merece la pena emprender mayores ensayos clínicos aleatorizados y controlados con placebo”.
Es decir, que ya en 2006 la comunidad científica conocía la posible utilidad del etanercept en el tratamiento del alzhéimer. El estudio mereció un editorial en la revista que lo publicó, Medscape General Medicine,
que subrayaba su carácter “altamente preliminar” y sus limitaciones,
como la ausencia de controles con placebo y de un estudio
farmacodinámico, pero que concluía: “No todos los días (o todos los
años) se ven datos tan prometedores en el tratamiento del alzhéimer como
los que se presentan en este artículo, y claramente se necesitan más
estudios”.
En años posteriores, Tobinick continuaba publicando nuevos datos favorables, como un seguimiento de los pacientes y nuevos casos,
también con resultados de mejoras cognitivas. A finales de la década
pasada, los antiinflamatorios no esteroideos y en concreto los
inhibidores de TNF-α, como el etanercept o el infliximab, ya estaban en el punto de mira de muchos investigadores del alzhéimer.
Conviene aclarar aquí algo que también se ha propagado estos días y
que no es cierto. Algunos comentarios han aventurado que el etanercept
no puede ser útil contra el alzhéimer porque no atraviesa la barrera
hematoencefálica, el muro que separa el sistema nervioso central del
resto del organismo. Pero algunos expertos piensan que el hecho de que
el fármaco no atraviese esta barrera no tiene por qué impedir una
posible acción beneficiosa: existen indicios de que un efecto antiinflamatorio en el sistema nervioso periférico puede reducir la inflamación en el cerebro.
En el caso del TNF-α, la neutralización de esta citoquina fuera del
cerebro podría reducir la cantidad de esta molécula que llega al propio
cerebro.
Sin embargo, todo ello había que tomarlo con extrema cautela: además
de que los datos de Tobinick no dejaban de ser anecdóticos (sin ensayos
clínicos rigurosos), si por algo se distingue la investigación
del alzhéimer es por la inmensa cantidad de cadáveres de fármacos
prometedores que ha dejado en el camino. En ratones y ratas se
ha logrado curar la enfermedad infinidad de veces. Pero en realidad los
ratones y las ratas no padecen alzhéimer, por lo que se trata de modelos
creados por los propios investigadores. Y dado que en realidad aún no
se conoce cuál es la patogénesis del alzhéimer, los modelos animales no
son réplicas verdaderas de la enfermedad, sino de algunos de sus
síntomas. Se han creado empresas motivadas exclusivamente por un fármaco
que curaba este falso alzhéimer en ratones. Y han cerrado empresas
cuando se comprobaba que este fármaco no hacía absolutamente nada contra
el alzhéimer real.

Modelo de alzhéimer en el cerebro de un ratón: placas beta-amiloides (rojo) entre las neuronas (verde). Imagen de NIH.
En el caso de los antiinflamatorios no esteroideos, muchos de ellos han curado el alzhéimer en ratones; ninguno de ellos ha funcionado en pacientes. También el etanercept y moléculas similares han mostrado eficacia en modelos animales, pero esto no es ni muchísimo menos una garantía de que servirán como fármaco.
Así las cosas, al mismo tiempo comenzaban a llegar otros datos no tan
positivos. Dado que el etanercept por su propia naturaleza es un
inmunosupresor, se reportaban casos de pacientes afectados por infecciones graves e incluso mortales por el uso de este medicamento contra la artritis reumatoide, lo que obligaba a la Agencia de Fármacos de EEUU a publicar una advertencia.
Esto tiene una implicación trascendental: el etanercept jamás será un fármaco para prevenir el alzhéimer.
Sencillamente, tratar a personas sanas con un inmunosupresor durante
largos periodos de su vida es algo que está fuera de toda discusión.
Por fin en 2015, el año en que la patente del etanercept expiró en Europa (no en EEUU), investigadores británicos emprendieron el primer ensayo clínico doble ciego, aleatorizado y controlado con placebos para evaluar el uso del fármaco contra el alzhéimer.
Se trataba de un estudio aún muy pequeño, con 41 pacientes de
alzhéimer, y en fase 2. La fase 1 de un ensayo clínico se centra en la
seguridad del fármaco, mientras que la fase 2 confirma estos datos de
tolerabilidad y empieza a valorar sus posibles efectos. Por cierto, y
aunque en EEUU Amgen se había mostrado reticente a los ensayos clínicos
del etanercept para otras indicaciones, este estudio fue financiado a
través de una ayuda de Pfizer al investigador principal, Clive Holmes.
Los resultados de tolerabilidad fueron positivos. Sin embargo, los de eficacia fueron decepcionantes: “No hubo cambios estadísticamente significativos en cognición, comportamiento o función global”,
escribían los autores del estudio. No había diferencias entre el
etanercept y el placebo. Lo cual suscitó una evidente pregunta: ¿y si
los resultados reportados por Tobinick solo eran un efecto placebo?
Aquí es donde las cosas empiezan a complicarse aún más. Por un lado,
el ensayo británico empleó etanercept por vía subcutánea, no espinal
como en los estudios de Tobinick. Pero los investigadores concluían: “El
presente estudio no debería verse como un apoyo al uso subcutáneo no
aprobado de etanercept para el tratamiento del alzhéimer. El etanercept tiene reconocidos efectos adversos potencialmente serios en la población”.
Al mismo tiempo, los resultados del estadounidense comenzaban a cuestionarse seriamente.
Tras ser amonestado por el Consejo Médico de California por conducta no
profesional, Tobinick se mudó a Florida, un estado permisivo, donde
montó una clínica en la que aseguraba tratar todo tipo de enfermedades
neurológicas –incluidas las no autoinmunes– mediante sus inyecciones.
Sin ensayos clínicos relevantes, Tobinick comenzaba a cargar a sus
pacientes altas sumas por tratamientos con etanercept. Se revelaba
además que el investigador no era un neurólogo, sino un internista que
antes se dedicaba a la depilación por láser. Al parecer, y después de
que sus tratamientos contra el alzhéimer fracasaran, Tobinick se centró
en otras enfermedades.
Y en todo esto, ¿dónde entra el lío con Pfizer que ha hecho correr tanta tinta física y digital en los últimos días? El pasado martes, el diario The Washington Post publicaba una exclusiva
según la cual, decía el titular, “Pfizer tenía pistas de que su fármaco
superventas podía prevenir el alzhéimer” y las ocultó al mundo. En el
texto, el periodista contaba que a sus manos había llegado un Power
Point en el que se mostraban datos de cientos de miles de reclamaciones
de seguros médicos que algunos investigadores de la compañía habían
cruzado en 2015, y que se presentaron a la dirección en 2018. Según
estos datos, de dos grupos iguales de 127.000 pacientes con alzhéimer y
otros tantos sin esta enfermedad, todos ellos afectados por artritis
reumatoide o dolencias similares, en el primer grupo (alzhéimer) 110
personas habían recibido etanercept, mientras que en el segundo (no
alzhéimer) eran 302.
La crítica a Pfizer se basa en que no hizo públicos estos datos. Lo
cual no implica que se mantuvieran en secreto: Holmes dispuso de ellos
para su ensayo clínico. Pero si la pregunta es si la comunidad
científica debería disponer de este tipo de datos, no creo que nadie
objete que la respuesta es sí; la comunidad científica siempre tiene y debe tener hambre de datos, por lo que ningún indicio sobra, ninguno está de más. Ahora bien, si la pregunta es si los datos de Pfizer eran realmente relevantes…
En primer lugar, los datos de Pfizer no son novedosos. En 2016 se publicó un estudio similar:
investigadores estadounidenses cruzaron datos de pacientes con artritis
reumatoide, con o sin alzhéimer, con o sin tratamiento con etanercept, y
concluyeron que “hay un riesgo mayor de alzhéimer en la población de
artritis reumatoide estudiada”, y que “el riesgo relativo de alzhéimer
entre los sujetos con artritis reumatoide era menor en los expuestos a
etanercept”.
En segundo lugar, ¿qué revelan en realidad estos datos? Exactamente
lo que dicen: que entre los enfermos de artritis reumatoide hay menos
casos de alzhéimer entre los tratados con etanercept. No hay en absoluto una relación causa-efecto demostrada, y correlación nunca significa causalidad;
nada descarta la posibilidad, por ejemplo, de que el etanercept, una
medicación con efectos adversos serios, se administre con más frecuencia
a los pacientes con un cuadro general menos grave. Para discernir entre
las posibles hipótesis alternativas y relacionar causas y efectos con
base científica son imprescindibles los ensayos clínicos rigurosos.
Por último, y dado que los datos se refieren exclusivamente a enfermos de artritis reumatoide, no
hay absolutamente nada en ellos que sugiera una utilidad del etanercept
contra el alzhéimer en personas sin artritis reumatoide. El único estudio riguroso que ha abordado esta cuestión hasta ahora, el pequeño ensayo de Holmes, fue negativo.

Estructura del TNF-alfa. Imagen de BQUB14-Jcanas / Wikipedia.
En resumen, ¿cuáles son las perspectivas de que se obtenga algo
válido del etanercept contra el alzhéimer? Desde luego, nada invita a
sospechar que este fármaco vaya a ser jamás la bala mágica contra el
alzhéimer. Como ya he dicho arriba, es impensable que se plantee su uso como medicamento preventivo.
Si acaso los enfermos de artritis reumatoide tratados con el fármaco
pudieran beneficiarse de un posible efecto secundario en este sentido,
bienvenido sea. Pero esto no aporta nada al resto de la población
general, ni siquiera a la población de riesgo por su perfil genético.
El propio artículo del Washington Post, excelentemente trabajado a pesar de su desafortunado titular click-bait, dice: “Ninguno
de los expertos entrevistados para esta historia dijo que tal
indicación fuera de etiqueta del Enbrel [etanercept] contra el alzhéimer
sería apropiada, dada la naturaleza muy limitada de los datos
hasta ahora. Ni creen que esta prescripción vaya a producirse de manera
significativa”.
En definitiva, si del etanercept, ya en el dominio público, o de sus
muchos fármacos biosimilares ya existentes, podrá obtenerse algo
positivo en el futuro contra el alzhéimer, solo el tiempo lo dirá;
siempre, naturalmente, que este tiempo se dedique a emprender múltiples
ensayos clínicos rigurosos. Que Amgen y Pfizer decidieran no abordar estos ensayos forma parte de su libre derecho como empresas.
Que no publicaran un conjunto de datos que no aporta nada novedoso y
cuya relevancia científica es relativamente escasa puede ser todo lo
criticable que a cada uno le parezca, por supuesto.
Pero tirar de esta anécdota para apoyar una causa general contra estas compañías o contra la Big Pharma
solo viene a demostrar una vez más que los pilares más fuertes en los
que se sostiene dicha causa general suelen ser el odio irracional y el
pensamiento conspiranoico. Que se alimentan solo de titulares, no de las noticias que van debajo. Y que por cierto, también son una industria muy rentable.
Soy periodista, biólogo y doctor en Bioquímica y Biología Molecular.
Antes de dedicarme al periodismo, en los años 90 trabajé en
investigación en el Centro Nacional de Biotecnología y publiqué 19
estudios científicos y revisiones. Como periodista de ciencia, fui jefe
de sección de Ciencias del diario Público, y entre mis colaboraciones
figuran medios como El País/Materia, El Huffington Post, ABC, Efe o BBVA
OpenMind, entre otros. En mis ratos libres también intento viajar y
escribir sobre viajes. He publicado tres novelas: 'El señor de las
llanuras' (Plaza & Janés, 2009), 'Si nunca llego a despertar' (Plaza
& Janés, 2011) y 'Tulipanes de Marte' (Plaza & Janés, 2014).
https://blogs.20minutos.es/ciencias-mixtas/2019/06/07/no-pfizer-no-ha-ocultado-al-mundo-un-farmaco-que-cura-o-previene-el-alzheimer-ii/?fbclid=IwAR1M2h0SlKypKGMpDRJmcdpho0lLU0xDyu9kEdV8VCDjT-BCO-2e_giFSeI
3.Piensa bien y acertarás: los casos de Pfizer e Isdin
Fronteras

En el periodo de una semana los grandes
medios de comunicación difundieron informaciones falsas en contra de
dos importantes laboratorios farmacéuticos: Isdin y Pfizer. Isdin
fue acusado de comercializar un producto de protección solar pediátrica
con un SPF menor al indicado. Pfizer fue acusado de ocultar pruebas que
indicaban que uno de sus fármacos previene el alzhéimer.
Cuesta
encontrar alguna razón coherente por la que estos laboratorios tendrían
interés en engañar con un factor de protección solar o en ocultar ni más
ni menos que un fármaco contra el alzhéimer. Sin embargo, estas
informaciones falsas fueron reproducidas en los principales medios de
comunicación en televisión, radio, prensa y redes sociales. Ante
informaciones tan descabelladas como estas, deberían saltar todas las alarmas de que estamos ante fake news. Sí, estamos ante fake news, pero muchos lo pasaron por alto.
Ni Isdin, ni ningún otro laboratorio, mienten acerca del factor de protección solar
Ningún producto cosmético puede salir al mercado indicando un factor de protección solar si antes no ha sido validado por las autoridades sanitarias.
Cualquier producto cosmético en el
que se indique un factor de protección solar (SPF), sea de la magnitud
que sea, ha tenido que certificarlo ante las autoridades sanitarias
mediante ensayos clínicos tipificados. En el caso de España, el
resultado de estos ensayos clínicos ha de ser validado por la Agencia
Española del Medicamento y el Producto Sanitario (AEMPS). Una vez
validados los resultados del ensayo clínico, el laboratorio puede
incluir en indicativo del SPF correspondiente en su producto. Estos
ensayos se hacen producto por producto, individualmente y en el producto
acabado.
Para certificar el SPF se hace un ensayo in vivo, el generalmente tipificado bajo la norma ISO 24444:2010 (equivalente al International Sun Protection Factor Test Method o método COLIPA). En este ensayo se cubre una zona de piel con el producto a evaluar a razón de 2 mg/cm2.
Se mide por cuánto se multiplica el tiempo de exposición a la radiación
UV hasta la aparición de enrojecimiento o eritema con y sin el producto
aplicado. La principal radiación responsable de las quemaduras
(eritemas) es la UVB, por eso el SPF es realmente una medida de protección contra la radiación UVB.
Así, un SPF 30 significa que se multiplica al menos por 30 el tiempo al
que la piel puede estar expuesta al sol sin sufrir quemaduras. Un SPF
50+, que actualmente es el mayor factor de protección solar, indica que
la protección ante las quemaduras dura por encima de 50 veces más que la
piel sin protección. Los productos pediátricos suelen tener SPF 50+.
La
validación por parte de la AEMPS y el coste del ensayo clínico, que no
es precisamente barato, es el mismo para cualquier SPF.
Para
certificar la protección frente a la radiación UVA, el llamado UVA-PF,
se hace un ensayo diferente, generalmente el tipificado bajo la norma
ISO 24443:2012 (equivalente in vitro al PDD, Persistent Pigment Darkening).
El PDD se calcula por medio del cociente entre la dosis mínima de UVA
necesaria para inducir un oscurecimiento pigmentario persistente de la
piel protegida por un producto de protección solar y la dosis mínima de
UVA necesaria para inducir el oscurecimiento mínimo de la misma piel sin
proteger. Si el cociente entre el SPF y el UVA-PF es de 1/3 o
inferior, el fabricante podrá incluir el indicativo de protección solar
frente al UVA. Este indicativo no es numérico, sino el del UVA rodeado
con un círculo.
La última semana de mayo de 2019, la Organización de Consumidores y Usuarios
(OCU), una organización privada cuyo objetivo es defender los derechos
del consumidor, envió una nota de prensa a los medios de comunicación
indicando que habían hecho un estudio con 17 productos de protección
solar pediátrica, de los cuales dos de ellos no llegaban al SPF indicado. El de los laboratorios Isdin fue el peor parado:
según la OCU, uno de sus productos con SPF 50+ solo llegaba a SPF 15.
La nota de prensa fue reproducida en los principales medios de
comunicación, acaparando la atención durante días.
Isdin hizo públicos los estudios y resultados que certifican que ese producto cumple con el SPF y con el UVA-PF indicados, que en su día fueron facilitados a la AEMPS. La OCU no hizo públicos sus estudios,
alegando que no podían desvelar la identidad de su laboratorio. Este
dato ya debería ser suficiente para que los medios de comunicación
decidiesen no publicar la nota de prensa. En cambio, la nota se publicó sin que nadie antes pudiese comprobar que ese estudio existía o que era veraz.
Si un cosmético es defectuoso,
causa algún tipo de alergia o reacción adversa, tenemos la sospecha de
que no protege del sol como debería, no tiene buen aspecto u olor…
debemos notificarlo. Debemos notificarlo directamente en la AEMPS a través de su servicio de cosmetovigilancia, o podemos notificarlo a personal sanitario, a los distribuidores del producto o en la farmacia.
Las farmacias tienen la obligación de notificar cualquier incidencia
tanto al laboratorio como a la AEMPS. A partir de ese momento se pondrá
en marcha un proceso de análisis del producto para detectar si se trata
de una alerta real, de una alerta concreta o bien de una alerta
extensible a un lote de productos defectuosos. Si se tratase de una alerta real, se procedería a la retirada inmediata del producto en todos los puntos de venta.
Si
un cosmético es defectuoso o tenemos la sospecha de que así lo sea, hay
que notificarlo primero y en exclusiva a las autoridades sanitarias, en
este caso la AEMPS. Lo que no hay que hacer es enviar una nota de
prensa a los medios de comunicación antes de que la AEMPS verifique si
estamos ante un producto defectuoso, ni siquiera antes de que la
AEMPS decida cuál es la mejor forma de proceder: enviar una circular a
los puntos de venta, crear una alerta para que la difundan los medios de
comunicación, retirada inmediata del producto, etc. Lo que ha hecho la OCU es precisamente lo que no hay que hacer. Se han saltado el procedimiento y han creado una alerta sin supervisión de la AEMPS. Para más inri, todo esto este disparate fue promovido y agitado por los medios de comunicación.
Pfizer no ocultó un medicamento contra el alzhéimer
El 4 de junio The
Washington Post publicaba que el laboratorio farmacéutico Pfizer tenía
pistas de que su fármaco superventas podía prevenir el alzhéimer y que
las ocultó al mundo. En pocas horas la prensa española reproducía el artículo acompañado de titulares desinformadores y demagógicos.
Aunque el cuerpo de la mayor parte de estos artículos era una
reproducción del original, algunos medios argüían sobre las posibles
razones que llevarían a Pfizer a ocultar tremendo descubrimiento: que si
la patente estaba a punto de expirar y no sería rentable, que es más
rentable la enfermedad que la cura… Razones absolutamente delirantes.
Obviando las cuestiones éticas, descubrir un fármaco que cura o previene el alzhéimer es, a todas luces, muy rentable.
El principio activo del medicamento Enbrel de Pfizer es etanercerp.
El etanercerp es una proteína quimérica que inhibe la acción de la
TNF-α, una molécula que produce el organismo que promueve los procesos
inflamatorios. Esta molécula se lleva comercializando desde 1998 para el tratamiento de la artritis reumatoide por una compañía que desde 2009 pertenece a Pfizer.
Desde hace años sabemos que uno de los síntomas del Alzhéimer es la inflamación,
pero desconocemos cuál es el papel de la inflamación en esta
enfermedad, y si su supresión palía sus síntomas o si frena su
progresión. Esta es una de las líneas de investigación. Es por ello que los antiinflamatorios, entre ellos el etanercerp y otra veintena de moléculas biosimilares a esta, se hayan estudiado como posibles fármacos contra el alzhéimer.
En 2006 se publicó un estudio piloto que evaluó el uso de etanercerp contra el alzhéimer. Aunque los resultados eran altamente preliminares, sí parecían prometedores. Más adelante se descubrió que estos antiinflamatorios curaban el alzhéimer en animales (al menos una réplica de la enfermedad) pero desgraciadamente no funcionaba así con humanos.
En 2015 se hizo el primer ensayo clínico doble ciego, aleatorizado y controlado con placebos, para evaluar el etanercerp contra el alzhéimer. Este estudio fue financiado por Pfizer. Los resultados de eficacia fueron decepcionantes, no distinguibles del placebo. La conclusión del estudio es que el etanercerp no cura ni previene el alzhéimer.
El periodista que escribió para The Washington Post relataba que había llegado a sus manos un power point en el que figuraban datos cruzados de compañías de seguros. Según estos datos, había una menor incidencia de alzhéimer entre personas con artritis reumatoide tratadas con etanercept, que entre personas con artritis reumatoide sin tratar. Se acusó a Pfizer de ocultar esta información. Pero ni siquiera estos datos se ocultaron: en 2016 ya se había publicado un estudio en
el que se cruzaban datos de pacientes con artritis reumatoide tratados
con etanercept relacionándolos con la incidencia de alzhéimer.
No
sabemos si hay una relación causa-efecto, ya que correlación no implica
causalidad. La realidad es que, de confirmarse esa relación
causa-efecto, solo sería aplicable a personas que padecen artritis
reumatoide y con carácter preventivo. No sería ni efectivo ni
conveniente para personas sin esta enfermedad. La razón es que los
efectos adversos del etanercerp sobre el sistema inmune hacen que sea
impensable administrar este fármaco como tratamiento preventivo del
alzhéimer. No se puede tratar a personas sanas con inmunosupresores como el etanercerp durante largos periodos de tiempo.
Pfizer
declaró ante los medios de comunicación que rechazó continuar esa línea
de investigación por razones estrictamente científicas. De hecho,
la evidencia científica de la que disponemos nos indica que,
desgraciadamente, etanercerp no sirve para prevenir el alzhéimer.
Algunos
medios de comunicación acusaron a Pfizer de ocultar datos por razones
económicas, en vista de que la patente sobre etanercerp estaba a punto
de caducar. Aunque ya hemos visto que no han ocultado ningún dato
relevante, tampoco es cierto que la patente estuviese a punto de caducar. La patente de este antiinflamatorio caducó en 2015, así que etanercerp ni siquiera es una molécula propiedad de Pfizer. Sin embargo, en EEUU la patente seguirá en vigor hasta 2028, ya que es propiedad de otra compañía, Amgen, que consiguió una prórroga. De
todos modos, si Pfizer o Amgen descubriesen un nuevo uso clínico de la
molécula, la patente podría extenderse hasta 20 años más, tiempo más que suficiente como para rentabilizar un descubrimiento de tal envergadura.

Consecuencias de estas fake news
No
es la primera vez que los medios de comunicación, la OCU y otras
empresas ponen en duda la efectividad y seguridad de los productos
cosméticos. Y no es la primera vez que tienen que desdecirse. Ya ocurrió con las cremas solares, con las BB cream, con las hidratantes… Tras analizar estos productos, con metodologías puestas en cuestión por asociaciones como Stanpa, la compañía publica un ranking. Ranking al que solo se puede acceder previo pago de la cuota de socio. Casualmente la “compra maestra” de esos rankings siempre es la de un cosmético de marca blanca, de la misma marca blanca.
Aun así, no podemos acusar a la OCU de mantener una relación comercial
interesada con la distribuidora de esa marca blanca porque no hay
pruebas de ello.
Una de las consecuencias es que el producto de marca blanca bate récord de ventas
y se agota en unos días. Otra de las consecuencias es que la OCU recibe
muchas visitas y atención por parte de todos los medios de
comunicación. Es una gran estrategia de propaganda.
Toda aquella información que corrobora un prejuicio (en este caso en contra de los laboratorios cosméticos) y que nos dice lo que queremos oír (que es tan bueno el cosmético más barato como el más caro) es una garantía de éxito mediático.
La realidad es que los productos cosméticos son seguros, funcionan y
que, salvo contadas excepciones, cuestan lo que valen. Pero la verdad no
genera tantos clics.
El caso reciente de la acusación pública de la OCU hacia los laboratorios Isdin es todavía más intolerable. Poner en cuestión la eficacia de los productos de protección solar tiene unas implicaciones sanitarias fatales. Según la Asociación Española Contra el Cáncer, actualmente tenemos unas muy buenas cifras de concienciación
sobre protección solar. Estas cifras peligran cada vez que los medios
de comunicación ponen en duda la eficacia de los productos de protección
solar. Que los medios de comunicación compartan notas de prensa
como las de la OCU, sin tan siquiera ponerse en contacto con expertos,
con el laboratorio, con la AEMPS, sin solicitar los estudios que
corroboran las acusaciones, es de una enorme irresponsabilidad.
Hay que considerar también las pérdidas económicas.
Por un lado para las farmacias y parafarmacias, que es donde se
comercializan los productos de Isdin. Por otro lado, Isdin es un
laboratorio cosmético muy focalizado en los productos de protección
solar. Precisamente esta oleada de desprestigio mediático llega en el
momento clave de la campaña de solares. Por poner un ejemplo, el salario
de los delegados comerciales de estos laboratorios está sujeto a
objetivos, con lo que el descenso en las ventas y las devoluciones
repercute directamente en el salario de estos trabajadores. Un descenso
en ventas en España, donde este laboratorio es especialmente fuerte,
repercutirá en los salarios y puestos de trabajo de muchos
profesionales, entre ellos un gran número de científicos. Han ido a dar
donde duele y cuando más duele, caiga quien caiga.
La OCU ha manifestado que los estudios sobre protectores solares que han hecho ya están en manos de la AEMPS. Hasta la fecha la AEMPS no ha iniciado ningún procedimiento de retirada de productos.
Lo más probable es que los estudios de la OCU no estuviesen bien
hechos, como ya ha ocurrido con anterioridad. También podría suceder que
hubiese un producto o lote de productos defectuosos. Sea como fuere,
esta no es la forma responsable de proceder, ni por parte de la OCU ni
por parte de los medios de comunicación.
Con respecto a Pfizer, parece que de momento no ha habido consecuencias económicas reseñables. Las acciones de la compañía
no se han visto afectadas por el incidente. La principal consecuencia
de todo esto es la imagen desgastada de los laboratorios farmacéuticos, y
con ello, de la investigación científica. De un caso anecdótico se ha
hecho un juicio generalizado hacia un sector entero.
Con respecto
a los medios de comunicación, muchos o no trabajan o trabajan mal. Y
quienes leen y comparten lo que estos publican, tienen muy dañado su detector de desinformación.
La
noticia de que Pfizer ocultó la cura del alzhéimer es tan rocambolesca
como los delirios de los charlatanes que afirman que se ha encontrado la
cura del VIH y que se oculta, o la cura del cáncer. Tan inverosímil
como que las farmacéuticas son las que crean las enfermedades y otras
conspiraciones de similar calibre.
Esta clase de noticias deberían hacer saltar todas las alarmas de detección de fake news. Ante la duda es recomendable preguntarse quién se beneficia.
Desde luego no hay beneficio posible para Isdin. Comercializar
protectores solares infantiles con menos SPF del indicado no beneficia a
nadie, y menos al laboratorio. Si Pfizer hubiese descubierto una cura
para el alzhéimer, ocultarlo sería la opción menos rentable. Sobre todo
sabiendo lo rentable que sería para el laboratorio que una de sus
moléculas sirviese para tal fin. Los únicos beneficiarios posibles son las empresas cuyos ingresos dependen del clic.
De ahí el título de este artículo: piensa bien y acertarás. Antes de
creer que los laboratorios farmacéuticos son el demonio, al menos
parémonos a pensar si hacer el mal les beneficiaría de algún modo. De lo
contrario, a cuento de qué iban a engañar. Es una sandez de tal
magnitud, que dejar escrito este párrafo me parece una forma de insulto.
Las fake news no solo circulan a través de estrafalarias páginas y grupos de las redes sociales, ni por whatsapp. Las fake news más peligrosas son las que llegan a los grandes medios de comunicación.
La
excusa de los medios de comunicación es la precariedad. Por eso se
reproducen noticias publicadas en The Washington Post aunque el titular
sea fehacientemente demagógico. Por eso se comparten notas de prensa de
la OCU aunque no aporten como fuente ni el estudio al que se refieren.
Todo esto aderezado con un titular jugoso que garantice un buen número
de clics. Mejor pan para hoy.
Ofrecer información de calidad
sobre estos temas de índole científica requiere tiempo y, sobre todo,
requiere conocimientos de partida. Si eso no se respeta, va a ser
imposible salir de esta crisis informativa y reconquistar la confianza.Solo aquellos que ofrecen información de calidad tienen porvenir. Para los demás, hoy pan y mañana suerte.
-
Para más información:
La ciencia del protector solar. Deborah García Bello. Fronteras, Cuaderno de Cultura Científica. Junio-agosto de 2018.
No, Pfizer no ha ocultado al mundo un fármaco que cura o previene el alzhéimer (I) y (II). Javier Yanes. Ciencias mixtas, 20 Minutos. 6 y 7 de junio de 2019.
Nota de la autora:
Deliberadamente en este artículo no se han incluido enlaces a las fake news publicadas acerca de Isdin o Pfizer a fin de no contribuir más a su difusión.
-
Sobre la autora: Déborah García Bello es química y divulgadora científica
-
No hay comentarios:
Publicar un comentario